При какой температуре плавится уксус
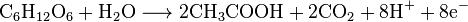
Уксусная кислота — органическое соединение, одноосновная карбоновая кислота состава CH 3 COOH. При обычных условиях представляет собой бесцветную жидкость с резким запахом. Температура плавления чистой кислоты несколько ниже комнатной температуры, при замерзании она превращается в бесцветные кристаллы — это дало ей техническое наименование ледяная уксусная кислота.
Название кислоты образована словом уксус, что происходит от лат. Acetum — кислое вино. По номенклатуре IUPAC она систематическую название етанова кислота, которая характеризует соединение как производную этана. Поскольку молекула кислоты имеет в своем составе функциональную группу ацетил CH 3 CO (условное обозначение Ac), ее формула также может записываться как AcOH. В контексте кислотно-основных взаимодействий символом Ac иногда сказывается ацетат-анион CH 3 COO — — в таком случае формула будет иметь запись HAc.
Взаимодействуя с металлами, щелочами и спиртами, уксусная кислота образует ряд солей и эфиров — ацетатов (етаноатив).
Уксусная кислота — один из базовых продуктов промышленного органического синтеза. Более 65% мирового производства уксусной кислоты идет на изготовление полимеров, производных целлюлозы и винилацетата. Поливинилацетат является основой многих ґрунтивних покрытий и красок. С ацетатной целлюлозы изготавливают ацетатного волокна. Уксусная кислота и ее эфиры важные промышленные растворители и экстрагенты.
Общие сведения
Уксусная кислота известна человечеству с древнейших времен. Уксус, 4-12% раствор уксусной кислоты в воде, как продукт ферментации вина получил широкое використування более чем 5000 лет назад, прежде всего как пищевой консервант. Древнегреческий врач Гиппократ использовал растворы кислоты в качестве антисептика, а также в составе настоек от многочисленных заболеваний, включая лихорадку, запоры, желудочные язвы, плеврит.
Уксусная кислота находится в низких концентрациях во многих растительных и животных системах. Она, в частности, синтезируется бактериями рода Acetobacter и Clostridium. Среди рода Acetobacter наиболее эффективно вид Acetobacter aceti.
В 1996 году американскими учеными было сообщено о наблюдении молекул уксусной кислоты в газо-пылевом облаке Стрелец B2. Подобное открытие впервые было осуществлено с применением интерферометрической оборудования.
Физические свойства
Уксусная кислота при стандартном состояния является бесцветной жидкостью с резким запахом. При замерзании при температуре 16,635 ° С, она превращается в прозрачные кристаллы (ледяная уксусная кислота).
| 25 ° C | 50 ° C | 75 ° C | 100 ° C | 110 ° C |
|---|---|---|---|---|
| 1,056 | 0,786 | 0,599 | 0,464 | 0,424 |
Уксусная кислота неограниченно смешивается с водой, образует значительное количество азеотропных смесей с органическими растворителями:
| Второй компонент | Температура кипения, ° C | Содержание кислоты,% | Содержание второго компонента,% |
|---|---|---|---|
| Гексан | 68,3 | 6,0 | 94,0 |
| Октан | 105,7 | 53,7 | 46,3 |
| Циклогексан | 78,8 | 9,6 | 90,4 |
| Бензол | 80,05 | 2,0 | 98,0 |
| Толуол | 100,6 | 28,1 | 71,9 |
| Етилбензен | 114,65 | 66 | 34 |
| Стирен | 116,8 | 85,7 | 14,3 |
| Пиридин | 138,1 | 51,1 | 48,9 |
| Тетрахлорметан | 76 | 98,46 | 1,54 |
| Хлоробензен | 114,7 | 58,5 | 41,5 |
| Нитроэтан | 112,4 | 30 | 70 |
Другие физические свойства:
- критическое давление 5,79 МПа;
- критическая температура 321,6 ° С;
- удельная теплоемкость 2 010 Дж / (кг · K) (при 17 ° С);
- поверхностное натяжение 27,8 · 10 -3 Дж / м² (при 20 ° С);
- коррозионная активность 10% -го водного раствора по отношению к ст. 3 2,97 г / (ч · м²) (20 ° С).
Получение
Синтез растворов уксусной кислоты (уксуса) проводится в основном методом ферментации, а для получения чистой кислоты, в значительных масштабах применяются методы карбонилирования метанола, окисления бутана и этаналя. Основным методом является получение из метанола.
Карбонилирования метанола
Возможность получения уксусной кислоты из метанола была открыта в немецком концерне BASF в 1913 году:
В 1938 году сотрудник BASF Вальтер Реппе продемонстрировал эффективность использования в качестве катализаторов карбонилов металлов VIIIB группы (группа 9), в частности, карбонила кобальта [Co 2 (CO) 8]. Первое полномасштабное производство с применением кобальтового катализатора было развернуто в 1960 году в Людвигсгафени, Германия.
В конце 1960-х в компании «Monsanto» разработали новый тип катализаторов на основе родия, которые имели значительно более высокую активность и селективность по сравнению с кобальтовым: даже при атмосферном давлении выход конечного продукта составлял 90-99%. В 1986 году этот метод приобрел «BP Chemicals» и передал его на совершенствование компании «Celanese».
В начале 1990-х «Monsanto» запатентовала использование нового, иридиевого, катализатора. Его преимущество заключалось в большей стабильности и меньшем количестве жидких побочных продуктов. «BP» приобрел права на этот патент и внедрил в производство под названием метод Cativa (англ. Cativa process).
Метод BASF
В производстве по методу BASF катализатором выступает карбонил кобальта [Co 2 (OH) 8], который in situ получают из йодида кобальта (II):
В реакционной системе образован карбонил активируют и в дальнейшем он находится в виде комплекса [Co (CO) 4] -:
На первой стадии исходный метанол взаимодействует с йодоводнем, который является сопутствующим продуктом синтеза карбонила, с образованием йодометану:
Йодометан реагирует с карбонил:
Впоследствии проводится карбонилирования что ведет к сложному ацилкарбонильного интермедиата:
Под действием йодид-ионов комплекс разлагается, высвобождая катализатор и ацетилйодид, который гидролизуется до уксусной кислоты:
Побочными продуктами в этом цикле является метан, этаналь, этанол, пропионовая кислота, алкильные ацетаты, 2-етилбутан-1-ол. На метан превращается около 2,5% метанола, а на жидкие побочные продукты — 4,5%. 10% монооксида углерода окисляется до диоксида:
Для реакции карбонилирования метанола чрезвычайно важны парциальные давления исходных веществ. Так, выход конечного продукта достигает 70% в зависимости от подачи монооксида углерода и 90% в зависимости от метанола.
Метод Monsanto
По методу Monsanto катализатором является дийододикарбонилродат [Rh (CO) 2 I 2] -, который синтезируют in situ из йодида родия (III) в водном или спиртовом среде.
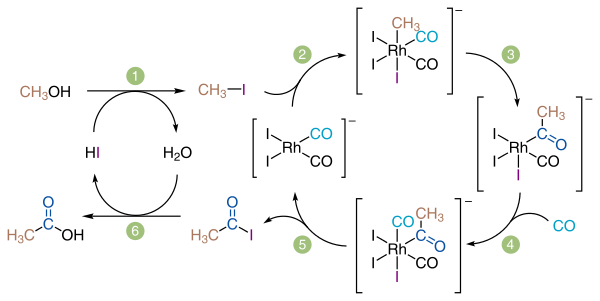
Компания «Celanese» усовершенствовала этот метод, дополнив его циклом оптимизации кислот, когда незначительная дополнительное количество уксусной кислоты в форме ацетат-ионов подавалась на катализатор и повышала его эффективность при низких концентрациях исходных соединений.
Синтез проводится при температуре 150-200 ° C и давлении 3,3-3,6 МПа.
Метод Cativa
Аналогичным метода Monsanto является метод Cativa. Здесь катализатором выступает заряженный комплекс [Ir (CO) 2 I 2] -.
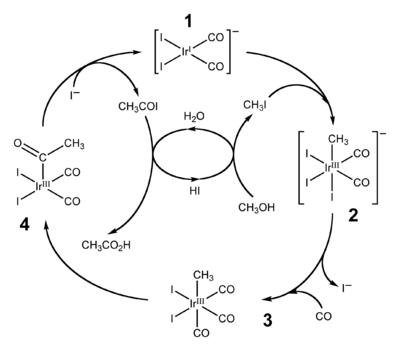
По сравнению с родиевым катализатором, иридиевый имеет и преимущества, и недостатки: так, окисления иридия йодометаном происходит в 150-200 раз быстрее, но процесс миграции метильной группы проходит в 10 5 -10 6 раз медленнее, к тому же образования побочного продукта метана для иридиевого катализатора выше.
Окисления этаналя
Прекурсором для получения уксусной кислоты служит этаналь, который синтезируют окислением этанола в присутствии солей серебра:
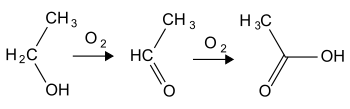
Окисление альдегида происходит по радикальному механизму с использованием инициатору:
Реакция проходит через стадию образования пероксоацетатного радикала:
Полученная пероксоацетатна кислота реагирует с ацетальдегидом с образованием ацетальдегидперацетату, который по механизму перегруппировки Байера — Виллигера разлагается на уксусную кислоту:
Побочным продуктом является метилформиат, который образуется в результате миграции метильной группы.
Катализаторами взаимодействий являются соли кобальта или марганца. Они также играют важную роль в уменьшении количества перацетат-радикалов в реакционной системе, тем самым предотвращая образование взрывоопасных концентраций:
Взаимодействия по этому методу проводятся при температуре 60-80 ° C и давлении 0,3-1,0 МПа. Преобразование альдегида в ацетатную кислоту обычно происходит с выходом более 90% и селективностью по кислотой более 95%.
Окисления углеводородов
Уксусная кислота может быть получена из бутана и легких фракций нефти. Этот метод является одним из самых распространенных благодаря низкой стоимости углеводородного сырья. В присутствии металлических катализаторов типа кобальта, хрома, марганца, бутан окисляется воздухом:
Основными побочными продуктами являются ацетальдегид и бутанон.
Ферментация
Некоторые бактерии, в частности, рода Acetobacter и Clostridium, производят кислоту в процессе своей жизнедеятельности. Использование человеком подобных ферментационных процессов известно еще с давних времен. Таким образом образуется низкоонцентрированных уксусная кислота, которая полностью удовлетворяет бытовые нужды.
К ферментативного производства привлекаются виды бактерий Acetobacter aceti и искусственно выведенные Clostridium thermoaceticum. Для подкормки бактерий используют сахаросодержащую сырье — глюкозу, ксилозу и т.п.:
Значительным преимуществом этого метода является полная экологичность производства.
Химические свойства
В газовой фазе между молекулами кислоты возникают водородные связи, поэтому они находятся преимущественно в димерних форме (также известные тетрамеры):
Кроме этого возможно образование гидратированного димера: молекулы сочетаются между собой только одним связью, а к свободным карбоксильной и гидроксильной групп присоединяются водородными связями по одной молекуле воды. Степень превращения в димерные структур увеличивается с повышением концентрации раствора и снижается с повышением температуры.
Уксусная кислота является типичной карбоновой кислотой, она участвует во всех реакциях, характерных для этого ряда соединений. В водном растворе кислота распадается и отдает ион H + молекулам воды, образуя структуру с двумя равными связями C-O:
Проявляя кислотные свойства, уксусная кислота взаимодействует с активными металлами, оксидами и гидридами металлов, металлоорганических соединений, аммиаком, образуя ряд солей — ацетатов.
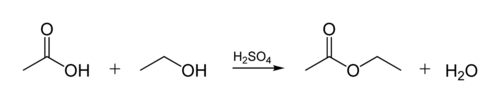
Органические ацетаты является эфирами — продуктами взаимодействия кислоты со спиртами:
Конденсацией кислоты с этен синтезируют винилацетата — промышленно важную соединение, мономер поливинилацетата:
При воздействии сильных обезвоживающих агентов (типа P 2 O 5) образуется уксусный ангидрид. Аналогичным результат при участии некоторых агентов хлорирования (тионилхлорида, фосгена) — тогда синтез ангидрида проходит через стадию получения ацетилхлорида.
Пропуская разогретую пару кислоты над катализатором (оксидами марганца, тория, циркония), можно синтезировать ацетон (с выходом около 80%):
При нагревании до 600 ° C уксусная кислота дегидратируется к Кётене — етенону:
Токсичность
Находясь в состоянии пара в воздухе, кислота повреждает глаза, нос и горло уже при концентрации более 10 мг / м³. Серьезные последствия наблюдаются при десятидневной повторяющейся действия загрязненной кислотой воздуха с содержанием до 26 мг / м³.
Низкоонцентрированных растворы уксусной кислоты (около 5%) могут раздражать слизистые оболочки. Концентрированная кислота в значительной степени повреждает кожу при контакте: в случае ее попадания, необходимо промыть пораженное место большим количеством воды или раствора пищевой соды. При проглатывании уксусной кислоты наблюдается боль в пищеводе и рту, это может привести к появлению тошноты и проблем с дыханием. В этом случае необходимо ополоснуть ротовую полость и обратиться к врачу.
Токсические дозы при потреблении кислоты человеком точно не известны. Полулетальные дозой для крыс является 3310 мг / кг, для кроликов — 1200 мг / кг. Потребление человеком 89-90 г чистой кислоты крайне опасно, а предельной численностью для ежедневного потребления является 2,1 г.
Применение
Применение уксусной кислоты достаточно разнообразное. В химической промышленности из нее производят пластические массы, различные красители, лекарственные вещества, искусственное волокно (ацетатный шелк), невоспламеняющуюся кинопленку и многие другие вещества. Соли уксусной кислоты — ацетаты алюминия, хрома, железа — применяют как протраву при окраске тканей. Уксусная кислота имеет широкое применение и в качестве растворителя.
В пищевой промышленности применяется как консервант, регулятор кислотности и вкусовая приправа; в Европейской системе пищевых добавок уксусная кислота имеет код E260.
Кислота применяется при солянокислотного обработке призабойной зоны пласта в качестве стабилизатора (с целью стабилизации продуктов реакции) от выпадения складновилучуваних гелеобразных соединений железа (осадка). В зависимости от содержания железа в кислотном растворе (от 0,01 до 0,5%) берут 1-3% уксусную кислоту. Для приготовления рабочих растворов используют как синтетическую кислоту, так и лесохимическую техническую очищенную.
Источник
Синонимы:
этановая кислота, метанкарбоновая кислота
Уксусная кислота является одной из самых важных органических
кислот.
История уксуса
Уксус является продуктом, который известен человечеству уже
более 7000лет.
Гиппократ описывал его использование в качестве внутреннего
и наружного средства.
Уксус являлся важным консервантом и пряностью. В древних
писаниях он упоминается как безалкогольный напиток для путешествий, охоты и
работы.
В течение многих веков раствор уксусной кислоты
использовался в качестве дезинфицирующего средства. Например, во время
смертельных эпидемий чумы им пропитывались защитные маски.
Получение уксуса в древности, вероятно явилось следствием
случайного открытия при ферментации виноградного сока в вино.
При алкогольной ферментации дрожжи превращают сахар в этанол
и углекислый газ. При этом емкости для брожения должны быть надежно защищены от
попадания воздуха. Иначе бактерии уксусной кислоты, в присутствии кислорода,
могут ферментативно окислить этанол до уксусной кислоты, и вино приобретет кислый
вкус.
Однако, при природном (естественном) ферментативном
окислении можно получить максимальную концентрацию не более 15% уксусной
кислоты, поскольку ферменты неэффективны при более высоких концентрациях. Они
практически убивают сами себя.
Существует много разных сортов уксуса, которые отличаются не
только концентрацией, но и вкусом.
Однако, основным компонентом у них всегда будет вода и уксусная кислота
(этановая кислота).
Структура и свойства уксусной кислоты
Это органическая кислота (карбоновая кислота), молекулы
которой имеют два атома углерода, связанных друг с другом простой связью.
Функциональная группа, как и все другие карбоновые кислоты,
представляет собой карбоксильную группу – COOH.
Физические свойства
- Молярная масса: 60,1 г/моль;
- Плотность: 1,044 г/куб.см;
- Температура плавления: 16,7 С;
- Температура кипения: 117,9 С.
Когда уксусная кислота растворяется в воде, примерно каждая
сотая молекула уксусной кислоты диссоциирует с образованием ацетат-иона.
Уксусная кислота имеет относительно высокую температуру
кипения (118 С) по сравнению с полярными веществами со сравнимой молярной
массой (например, 1-пропанол закипает при температуре 97 С). Причиной этого
является способность молекул уксусной кислоты образовывать две «взаимные»
водородные связи через свои карбоксильные группы. Полученные димеры возникают
из двух молекул уксусной кислоты, которые ведут себя как молекулы с двойной
молярной массой. Следовательно, для переноса этих димеров в газовую фазу
требуется большее количество энергии, что и характеризуется «повышенной»
температурой кипения.
Химические свойства
Этановая кислота – едкая, бесцветная, прозрачная, очень
гигроскопичная (влагопоглощающая) жидкость.
Безводную уксусную кислоту называют ледяной уксусной
кислотой. Название происходит от того, что чистая уксусная кислота затвердевает
до ледяных кристаллов уже при 16,7 C.
Этановая кислота смешивается с водой, эфиром, хлороформом,
этанолом и другими спиртами в любом соотношении.
Уксусная кислота является слабой кислотой. Это означает, что
она не полностью реагирует с водой, образуя ацетат-ионы и ионы водорода.
Благодаря полученным свободно подвижным ионам раствор
этановой кислоты является электропроводящим.
Уравнение реакции по Аррениусу:
Уравнение реакции по Бренстеду-Лоури:
Уксусная кислота полностью окисляется на воздухе с
конвекцией тепла в воду и углекислый газ.
Обычные металлы, такие как магний, кальций, цинк или железо, растворяются в разбавленной уксусной кислоте с образованием водорастворимых ацетатов и выделением водорода.
Реакции
Уксусная кислота образует соли (ацетаты).
Например, свинец образует токсичный, сладкий на вкус ацетат
свинца (свинцовый сахар). В древние времена римляне использовали свинцовые
сосуды в качестве кухонной утвари, а на керамические изделия наносили свинцовую
глазурь. Кислая пища или напитки способны растворять свинец. На основании
археологических исследований можно говорить о том, что хроническое отравление
свинцом в то время было, по-видимому, очень распространенным явлением.
Соли неорганических кислот реагируют с карбонатами и другими
солями.
Типичная реакция уксусной кислоты – образование эфира.
Производство
Классическим производством уксусной кислоты является процесс
ферментации, при котором бактерии Acetobacter превращают этанол (спирт) в
уксусную кислоту (уксуснокислое брожение). Исходными продуктами могут выступать
вино, пиво или солод.
Бытовой уксус состоит из ферментативного уксуса или
разбавленного синтетического уксуса с содержанием 5-10% уксусной кислоты.
Промышленное
производство
Наиболее важным промышленным синтезом уксусной кислоты
является каталитическая конверсия метанола с монооксидом углерода под давлением
(процесс Монсанто).
Помимо этого, уксусную кислоту также можно получить путем
окисления ацетальдегида воздухом или кислородом с использованием ацетата
марганца в качестве катализатора или путем частичного окисления других
углеводородов.
Помимо этого, этановую кислоту также можно получить другими
способами.
1. При каталитическом окислении в бутане с атмосферным
кислородом образуется уксусная кислота в смеси с многочисленными другими
полезными органическими соединениями (включая муравьиную кислоту).
2. Реакция этина (ацетилена) с этаналом (ацетальдегид) использовалась,
начиная с 1914 года.
В результате получался сырой уксус (технический уксус) с
концентрацией до 95%.
3. Возможно извлечь этановую кислоту из метанола и окиси
углерода.
Приготовленная таким образом уксусная кислота в основном
используется для приготовления различных сложных эфиров этановой кислоты,
которые из-за своего фруктового запаха используются в парфюмерии.
Использование
Только около 3% производимой во всем мире уксусной кислоты
используется в качестве пищевого уксуса (5% содержание уксусной кислоты) или
уксусной эссенции (25%).
Большая часть уксусной кислоты превращается в винилацетат,
из которого получают поливинилацетат. Он используется в качестве связующего для
красок и лаков, в бумажной и текстильной промышленности, а также в качестве
растворителя для клеев.
Другая значительная часть уксусной кислоты превращается в
уксусный ангидрид. Он может быть получен путем взаимодействия с ацетатом
целлюлозы (ацетилцеллюлоза), который затем перерабатывается в текстильные
волокна («искусственный шелк»), оправы для очков, сигаретные фильтры и другие.
Около 5-10% мирового производства уксусной кислоты
используется в качестве растворителя при производстве терефталевой кислоты,
которая затем перерабатывается в полиэтилентерефталат.
Соли уксусной кислоты используются в качестве пищевого
консерванта. Это ацетат натрия (E 262), ацетат калия (E 261) и ацетат кальция
(E 263).
Сама уксусная кислота используется в качестве подкислителя
для пищевых продуктов (E 260).
В быту уксусная кислота может использоваться для удаления
известкового налета:
А при стирке белья небольшое количество уксуса является
дешевой и экологически чистой заменой кондиционера для белья.
Воздействие на организм человека
Концентрированная уксусная кислота оказывает сильное
коррозионное воздействие на глаза, кожу и слизистые оболочки.
Порог чувствительности к запаху очень низкий – от 1 до 5
частей на миллион. Что обычно предотвращает вдыхание опасных для человека
концентраций этой кислоты.
Длительное вдыхание 100 ppm может вызвать отек легких.
Следует отметить, что попадание даже пищевого уксуса в глаза
может вызвать повреждение глаз. При попадании, следует незамедлительно промыть
глаза большим количеством воды.
Техника безопасности при работе с уксусной кислотой
При работе с концентрированной уксусной кислотой требуются
защитные очки и перчатки. Если в помещении не используются принудительные системы
кондиционирования, то работы должна выполняться в вытяжном шкафу.
Концентрированная чистая уксусная кислота (ледяная) – это
легковоспламеняющаяся гигроскопическая жидкость, которая легко испаряется. С
воздухом пары могут образовывать взрывоопасную смесь!
Купить уксусную кислоту
Источник